植物多酚是一种天然有机化合物,在自然界储量丰富。植物多酚具有特殊结构,因而容易与蛋白质结合,具有自由基清除功能,而且能够抵抗紫外线等多种功能而在畜牧业、食品和医学领域中得到广泛应用。微量金属元素是维持机体正常生命活动的必须物质,在多种生理生化过程中发挥着重要的作用。由植物多酚和金属离子络合组成的金属-多酚网络具有独特的多种生物功能而引起广泛关注,特别是在疾病诊断和治疗方面得到了广泛的研究。天然多酚类化合物迷迭香酸(RA)具有良好的抗肿瘤活性。然而,以低 pH 值和谷胱甘肽(GSH)水平升高为特征的独特肿瘤微环境增强了肿瘤对使用迷迭香酸的单一抗肿瘤治疗模式的耐受性,导致疗效不理想。RA 具有与金属元素配位的能力。为解决上述单一治疗模式的效果限制,构建一种自组装纳米复合材料Fe-RA。在肿瘤微环境下,Fe-RA 纳米复合材料可发挥类过氧化物酶(POD)的酶活和 GSH 的耗竭特性,产生大量羟自由基(-OH),破坏肿瘤细胞的抗氧化防御系统。此外,由于渗透性和滞留效应(EPR)增强,Fe-RA 可将 Fe2+ 更大程度地转运至肿瘤细胞,增加细胞内铁含量。造成肿瘤细胞铁代谢失衡,促进细胞铁嗜酸性变。同步辐射 X 射线吸收光谱(XAS)和高分辨质谱(HRMS)的研究结果证明,铁离子和RA络合是成功的。密度泛函理论(DFT)解释了其 POD 类酶活性的高效催化机理以及与 GSH 的反应原理。论文以“Self-assembled Fe-phenolic acid network synergizes with ferroptosis to enhance tumor nanotherapy”在国际期刊《Small》(IF=13.3)上发表。该论文通讯作者是伟德国际1946源于英国王显祥教授,农学院特用植物系陈银银老师为第一作者。
铁死亡是一种不同于细胞凋亡、自噬、坏死等的,受调控的细胞死亡方式。细胞内铁依赖性、毒性过氧化物的过度累积和细胞膜上高表达的不饱和脂肪酸等是细胞发生铁死亡的重要标志。Fe-RA金属-多酚网络通过增强渗透性和滞留效应,引起肿瘤细胞铁代谢失衡,促进细胞铁死亡。深入研究其分子机制发现,Fe-RA能够降低抗氧化酶谷胱甘肽过氧化物酶4(GPX4)和System Xc-的表达,影响NRF2/P62/Keap1蛋白通路,削弱胞内还原物GSH的合成,增加肿瘤细胞对铁下垂的敏感性,最终导致铁死亡的发生。该研究利用合成的铁-多酚网络在增强催化活性的基础上,结合肿瘤微环境的特点,协同细胞铁死亡,从而实现了对肿瘤的高效治疗。
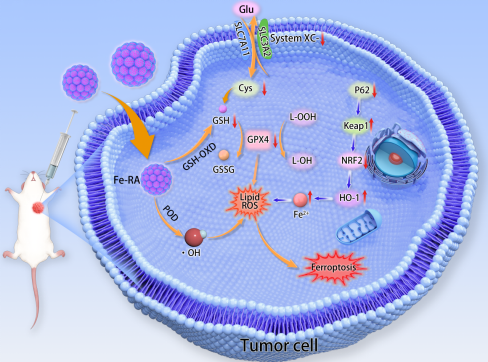
图1 Fe-RA 诱导肿瘤细胞铁死亡治疗癌症的机理示意图
本研究得到四川省科技计划项目、国家自然科学基金,以及伟德国际victor1946团队建设双支撑计划基金-创新团队项目和四川省中医药重点团队建设项目等项目的经费资助。
论文链接:https://doi.org/10.1002/smll.202402073